口服版司美格鲁肽终于在国内获批,但适应证仅限于二型糖尿病。
1月26日,国家药品监督管理局政务服务门户网站发布的2024年01月26日药品批准证明文件送达信息显示,诺和诺德的GLP-1受体激动剂司美格鲁肽片获批,批准日期为1月23日,共有两个批准文号。
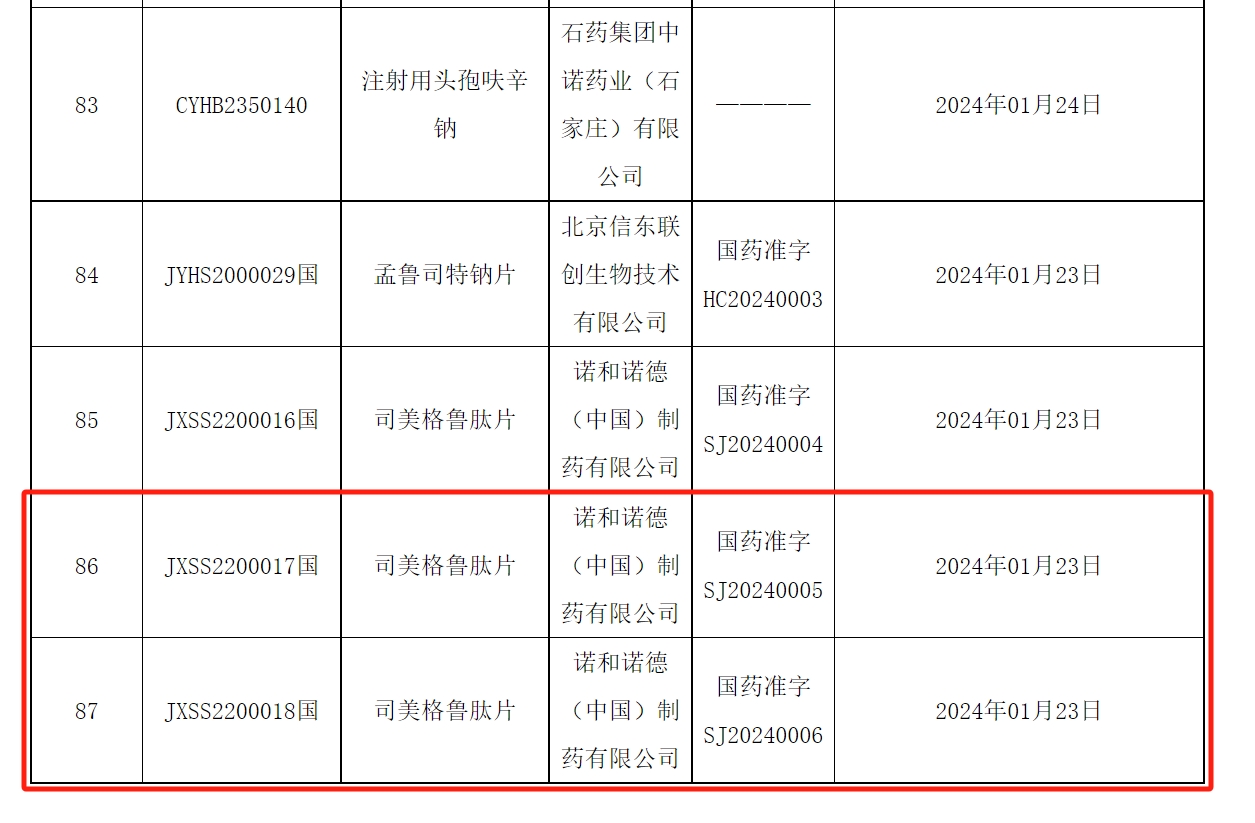
26日晚些时候,诺和诺德方面向澎湃新闻确认了上述获批消息,称司美格鲁肽片的获批标志着GLP-1类药物将进入口服时代。此前,诺和诺德的司美格鲁肽已经在国内获批用于2型糖尿病治疗,商品名为诺和泰,但剂型为针剂。诺和诺德方面介绍,此次获批的片剂商品名为诺和忻,同样用于成人2型糖尿病治疗。
口服版GLP-1药物获批用于糖尿病治疗
2023年以来,以司美格鲁肽为代表的GLP-1药物在全球走红,因为其强大的减重功效,被部分人称为“减肥神药”。目前,国内已经有多款GLP-1类药物获批,但都是需要患者注射使用的针剂,此次获批的司美格鲁肽为口服片剂,是国内首个获批上市的口服GLP-1受体激动剂。在中国之前,诺和诺德的口服版司美格鲁肽已经在美国、欧洲、日本等多个国家及地区获批上市。
剂型的变化有望提高患者的用药便利性和依从性,但另一个问题是,司美格鲁肽作为一种多肽类药物,口服经过胃肠吸收后往往会影响吸收。对于这一难题,诺和诺德中国称,借助“SNAC吸收促进剂”创新技术,司美格鲁肽片突破了这一技术壁垒。SNAC的促吸收作用可将口服给药途径的司美格鲁肽分子生物利用度提高约100倍。
值得关注的是,诺和诺德司美格鲁肽片在国外已经获批用于减重,那么这一适应证何时会在国内获批?目前,诺和诺德并未公布片剂的相关信息。不过,针剂版司美格鲁肽已在国内递交上市申请,并获国家药监局受理。
国产口服GLP-1药物有哪些在研?
作为带着“神药”光环的当红炸子鸡,GLP-1药物领域入局者不断,仅国内就包括华东医药(000963),恒瑞医药(600276)、丽珠集团(000513)、通化东宝(600867)、信达生物(1801.HK)、石药集团(1093.HK)等上市公司。
当前,GLP-1赛道竞争主要集中在靶点、适应证、剂型、用药频率等多个方面。围绕口服剂型,诺和诺德在中国已拔得头筹,但后方竞争者依然众多。
同为跨国药企的礼来拥有一款名为 Orforglipron的口服 GLP-1激动剂,已处于三期临床阶段,走在众多口服药物研发的前列。1月11日,据CDE临床试验登记与信息公示平台显示, 国内启动新一项三期临床ACHIEVE-5 试验,试验针对的是二型糖尿病。
华东医药已经有利拉鲁肽这一款GLP-1药物,此前在国内获批治疗糖尿病和减重。华东医药在2023半年报提到,其自主研发的口服小分子GLP-1受体激动剂HDM1002糖尿病适应证已于2023年5月首获中美双IND(新药临床试验)批准,并于2023年6月初实现首次人体试验首例受试者用药。肥胖适应证的中国IND申请已于2023年6月递交。
需要注意的是,礼来、华东医药的口服GLP-1与诺和诺德的有所不同,并非多肽药物,而是小分子药物。相比多肽药物,小分子药物口服时在吸收率方面表现或更好。
千亿疫苗巨头智飞生物(300122)此前拟收购的宸安生物除了布局有GLP-1/GIP双靶点受体激动剂,在研管线也包括口服司美格鲁肽片,不过仍位于临床前阶段;跨国药企巨头阿斯利康此前宣布与国内的诚益生物就ECC5004达成独家许可协议。根据当时披露的信息,ECC5004正是处于临床研究阶段的每日一次口服GLP-1受体激动剂(GLP-1),用于治疗肥胖症、2型糖尿病和其他心血管代谢疾病。
恒瑞医药产品管线也包括口服GLP-1药物HRS-7535,目前处于二期临床阶段。信立泰(002294)自主研发的SAL0112片(体重管理适应证)在2022年8月也获批开展一期临床试验。2023年10月,信立泰在投资者互动平台曾提到,112的目标适应证包括2型糖尿病、成人肥胖患者或超重患者的体重管理,目前处于一期临床研究阶段,预计明年进入二期临床。
(责任编辑:谭梦桐)





